HIV暴露前预防(PrEP)和抗逆转录病毒治疗(ART)是成人预防HIV感染和治疗疾病的主要成功选择。
与成人一样,婴儿也容易感染艾滋病毒和相关疾病。感染艾滋病毒且未经治疗的孕妇可能会让婴儿在子宫内或分娩后期或通过母乳喂养时将这种病毒传染给婴儿。
传播方式和初始感染时间会影响病毒的浓度(也称为病毒载量),从而影响婴儿的疾病结果。
因此,需要估计初始感染的时间并了解每个病例的初始感染时间,以便继续研究感染时间未知的婴儿群体中的艾滋病毒发病机制。
人类生物学DaraLehman博士和来自MatsenGroupFredHutchinson癌症中心公共卫生科学的第一作者Magdalena“Maggie”Russell创建并训练了一个数学模型,用于在婴儿感染史未知的情况下估计婴儿感染时间。
这项研究最近发表在《Plos Pathogens》上,将有助于定义婴儿的艾滋病毒疾病,并帮助确定何时应开始干预措施以及哪种类型可能最有效。
在成年人中,艾滋病毒多样性或独特病毒基因组的丰富度随着时间的推移而增加。这种多样性可以通过对病毒复制和感染其他细胞所必需的艾滋病毒基因进行测序来确定。
随着时间的推移,艾滋病毒多样性的增加归因于用于复制病毒基因组的容易出错的机制。利用这些知识,研究人员表明,使用HIV多样性测量作为输入数据的数学模型可以帮助估计感染史未知的病例的初始HIV感染时间,即仅在个体中测量的HIV序列多样性需要一个时间点来估计感染时间。
雷曼实验室试图使用类似的方法专门预测婴儿而不是成人的感染时间。为了生成这个模型,他们利用了1992年至2002年间在肯尼亚感染艾滋病毒的孕妇群体——当时ART尚未成为肯尼亚的标准护理方法。
出生后,对婴儿进行常规的艾滋病毒检测,在艾滋病毒检测呈阳性后,收集了额外的样本,通过对两个基本艾滋病毒基因内的三个不同区域进行测序,可以随着时间的推移测量艾滋病毒的多样性。
在该组中,一半婴儿在子宫内被感染,另一半在出生后被感染。与成人的艾滋病毒感染一样,婴儿的艾滋病毒多样性通常会随着时间的推移而增加。在与病毒载量、传播类型(子宫内感染、分娩时或后来通过母乳喂养)、免疫细胞监测等多个变量进行额外比较后,研究人员发现“HIV多样性中的这种积累速度,因个体、基因区域和感染模式而异,但不因设定点病毒载量或CD4+T细胞下降率而异”。
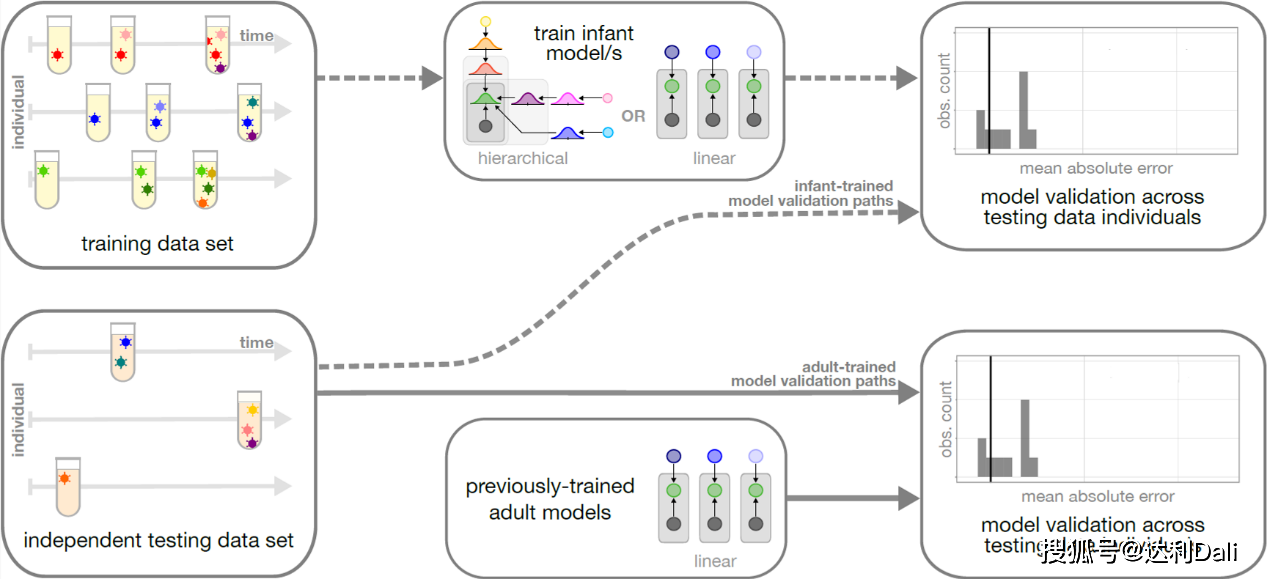
预测婴儿感染艾滋病毒时间的模型是根据已知的感染史和艾滋病毒多样性数据进行训练。
研究人员还将婴儿特定数据集和婴儿特定模型与针对成人艾滋病毒感染开发的数据集和婴儿特定模型进行了比较。
Russell表示:“我们的工作表明,与成人感染相比,儿童感染中的HIV序列多样化率似乎更高,”。
“这一发现提出了一个问题:为什么不同年龄组之间的多样化率存在如此大的差异。了解导致这种差异的潜在机制可以为理解儿科感染中艾滋病毒发病机制的差异提供有价值的见解。”
换句话说,随着时间的推移,与成人相比,其他因素可能会增强艾滋病毒,从而在婴儿中产生更多的艾滋病毒多样性。
“总之,这项研究对该领域做出了一些令人兴奋的贡献。首先,我们对未经治疗的儿科感染随时间推移的HIV序列多样化提供了新的见解,这一领域尚未得到充分研究,并且与成人的HIV序列多样化不同。”
婴儿艾滋病毒感染的这一特征对于了解如何制定有效的策略来预防和治疗感染至关重要。
Russell继续说道:“其次,我们创建了模型来估计艾滋病毒感染儿童的感染时间。虽然成人有艾滋病毒感染时间模型,但我们的婴儿模型填补了空白,并将有助于估计先前未知感染史的儿童的艾滋病毒感染时间,这在儿科艾滋病毒研究中非常重要。”
了解感染时间还可以指导如何治疗艾滋病毒感染以限制婴儿患病,以及为什么子宫内婴儿的早期感染会导致更多致病性疾病的结果。这些贡献有助于了解婴儿艾滋病毒感染以及下一代预防和治疗方案。
